Производство аммиака
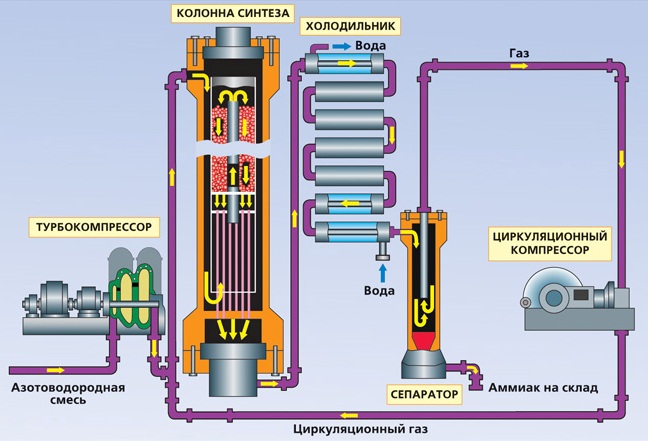
I. Сырьё: азотоводородная смесь (3VН2 + 1VN2)
II. Вспомогательный материал:
1) катализатор (пористое железо); 2) топливо; 3) вода.
III. Основной химический процесс:
N2 + 3Н2 = 2NН3 + 92кДж
(t = 450-500 0С, р = 15*106 Па)
IV. Побочные процессы: нет
V. Технологические принципы:
1) принцип непрерывности (циркуляционный);
2) принцип утилизации теплоты реакции;
3) принцип противотока;
4) принцип использования отходов производства.
VI. Технологические процессы:
1) тепловые (нагревание смеси N2 и Н2) (охлаждение NН3)
2) гидродинамические (перемещение газов и жидкостей по трубам,
смешивание газов, очистка газов);
3) диффузионные (ректификация, т.е. разделение NН3 и N2, Н2);
4) химические (см. пункт III, горение топлива)
VII. Основной продукт: аммиак
VIII. Побочные продукты: нет.
IX. Отходы производства:
1) Н2 и N2, которые снова идут на синтез аммиака;
2) продукты горения топлива.
Х. Охрана окружающей среды:
герметичность трубопроводов, по которым аммиак поступает на склад,
а Н2 и N2 – в колонну синтеза.
XI. Технико – экономические показатели:
1) W(NН3) выхода – 10-20%
2) производительность одной колонны в сутки – 1000 – 2000т.
3) замена катализатора – через 5-6 лет.
XII. Особенности технологического процесса: азотоводородная смесь
получают конверсией метана:
1. СН4 + Н2О(r) = СО + 3Н2 - 211 кДж
2. 2СН4 + О2 = 2СО + 4Н2 + 70кДж
3. СО + Н2О(r) = СО2 + Н2 + 38 кДж
Направление движения азотоводородной смеси в колонне синтеза выбирают таким образом, чтобы максимально использовать теплоту реакции и предохранять наружные стенки аппарат от нагревания.
Образующийся аммиак (10-20%) отделяют сжижением, возвращая непрореагировавшую азотоводородную смесь в колонну синтеза. Процесс непрерывный, циркуляционный.
Дополнительная информация: для синтеза аммиака применяют давление от 15 до 100 МПа.
В зависимости от применяемого давления различают 3 способа производства синтетического аммиака: низкого (10-15 МПа), среднего (25-30 МПа), высокого (50-100 МПа) давления. Наиболее распространён средний.
